KPV
Il KPV ha una potente attività antinfiammatoria nel sistema nervoso centrale, nel tratto gastrointestinale, nei polmoni, nel sistema vascolare e nelle articolazioni.
$4.10
◐ Prezzo pieno su WhatsApp!
◐ MOQ: 10 pezzi
◐ Impianto di produzione di peptidi
◐ Implementazione degli standard CGMP
◐ ISO9001 E ISO14000
CONDIVIDI QUESTO
Navigazione tra le informazioni sui prodotti
Struttura KPV
- Sequenza:Lys-Pro-Val
- Numero CAS:67727-97-3
- Formula molecolare:C16H30N4O4
- Peso molecolare: 342,43 g/mol
Che cos'è il KPV?
KPV è un frammento peptidico C-terminale dell'ormone stimolante gli α-melanociti (α-MSH). È uno dei numerosi derivati peptidici corti dell'α-MSH che sono stati testati per determinare se mantengono proprietà fotoprotettive, attività anti-ischemica, effetti sessuali o benefici sul comportamento alimentare e sull'omeostasi energetica simili.
Il KPV è costituito da lisina-prolina-valina e ha notevoli proprietà antinfiammatorie; il peptide è attivamente studiato come potenziale terapia per le malattie infiammatorie intestinali. È stata dimostrata una potente attività antinfiammatoria nel sistema nervoso centrale, nel tratto gastrointestinale, nei polmoni, nel sistema vascolare e nelle articolazioni e, poiché il KPV è un peptide di piccole dimensioni, può essere somministrato in vari modi, tra cui per via orale, endovenosa e transdermica.
Effetti KPV
Infiammazione intestinale
Forse il risultato più importante della ricerca sul KPV è che il peptide riduce l'infiammazione intestinale. In un modello murino di malattia infiammatoria intestinale (IBD), il KPV ha mostrato risultati solidi nel ridurre gli infiltrati infiammatori, l'attività della MPO e l'evidenza istologica complessiva dell'infiammazione; inoltre, i topi trattati con KPV nello studio si sono ripresi più velocemente e hanno guadagnato più peso rispetto ai topi trattati con placebo.
Ulteriori studi sul meccanismo di rilascio del KPV hanno dimostrato che il caricamento del KPV su nanoparticelle funzionalizzate con acido ialuronico aiuta a dirigere gli effetti infiammatori del peptide nei siti appropriati all'interno dell'intestino. In modelli murini, questo accelera la guarigione della mucosa e riduce l'infiammazione abbassando fortemente il TNF-α. Per molti versi, il KPV è un approccio più efficace e mirato per ridurre l'infiammazione delle IBD senza influenzare il TNF-α in altre parti dell'organismo. La modifica del KPV ha il vantaggio di aumentare la biodisponibilità orale del peptide. Questo non aumenta l'efficacia del peptide, ma influisce sulla potenza e sulla dose totale necessaria per ottenere l'effetto.
La KPV sembra essere efficace solo nei casi di infiammazione eccessiva. Ha un effetto minimo o nullo sui tessuti normali. Ciò è dovuto, almeno in parte, al fatto che il KPV entra nelle cellule del colon attraverso proteine di trasporto che non sono regolate in situazioni infiammatorie. Ciò suggerisce che il KPV può essere un efficace farmaco profilattico o di mantenimento per le IBD. È sicuro da assumere anche durante il periodo di riposo perché non ha alcun effetto. Il Prof. Didier Merlin, che ha condotto una serie di studi sui potenziali benefici gastrointestinali del KPV, ha recentemente scoperto che il peptide entra nelle cellule del colon attraverso la PepT1, una proteina canale che viene espressa in quantità reale nell'intestino solo durante gli stati infiammatori. Questo spiega perché il KPV è più efficace in un ambiente già infiammato. Inoltre, suggerisce una nuova modalità di somministrazione dei farmaci che può essere applicata a un'ampia gamma di patologie. Mirando alle proteine che sono alterate nelle condizioni di malattia, anche se non sono direttamente responsabili della malattia, è possibile concentrare l'attività di un farmaco su determinate regioni. In questo modo si potrebbe ridurre il dosaggio di farmaci con gravi effetti collaterali e sviluppare farmaci che, pur non essendo efficaci di per sé, hanno un potente effetto terapeutico nel giusto stato di malattia.
KPV come antinfiammatorio generale
Già nel 1984, studi condotti su conigli hanno dimostrato che il KPV è un potente antinfiammatorio e antipiretico (riduce la febbre). Tuttavia, in questo caso, il KPV era meno potente della molecola α-MSH intatta. Ciò indicava agli scienziati dell'epoca che il KPV mancava di alcune parti della molecola α-MSH necessarie per una piena attività antipiretica [5]. Seguirono decenni di ricerche su varie forme modificate di α-MSH.
Forse la più grande lezione appresa da questi test è che sia l'α-MSH che diversi suoi analoghi riducono l'infiammazione in un'ampia gamma di malattie. Ad oggi, queste molecole sono state testate nella febbre, nella dermatite da contatto irritante e allergica, nella vasculite, nella fibrosi, nell'artrite e nelle infiammazioni di occhi, cervello, polmoni e tratto gastrointestinale. In tutti i casi, l'alfa-MSH è l'agente antinfiammatorio più efficace. Purtroppo, ha un effetto collaterale importante: provoca la pigmentazione della pelle. Il KPV, invece, non ha questo effetto collaterale. Sebbene il KPV non sia efficace come l'α-MSH intatto, la sua mancanza di effetti collaterali significa che è teoricamente possibile aumentarne i livelli per ottenere l'effetto desiderato nella maggior parte dei casi.
Le differenze di potenza sono risultate al massimo minime, poiché la maggior parte degli effetti antinfiammatori dell'α-MSH è in realtà dovuta alla frazione KPV. È interessante notare, tuttavia, che la molecola madre sembra essere maggiormente in grado di inibire le risposte infiammatorie tardive. Ad esempio, nella dermatite da contatto, α-MSH previene meglio le reazioni infiammatorie allergiche fino a 2 settimane dopo l'esposizione iniziale. Ciò suggerisce che l'α-MSH possa influenzare qualche aspetto della regolazione immunitaria non legato alla risposta infiammatoria immediata [7]. Quale sia questo processo è ancora in fase di definizione.
Questa figura mostra il gonfiore dell'orecchio dovuto alla dermatite da contatto a 24 ore (sinistra) e a 2 settimane (destra). Si noti che a 24 ore la co-somministrazione di KPV con lo stimolo è quasi altrettanto efficace della co-somministrazione di α-MSH con lo stimolo. Tuttavia, a 2 settimane, l'esposizione all'irritante senza la co-somministrazione del peptide ha provocato un rigonfiamento molto minore di α-MSH rispetto a KPV.
Guarigione delle ferite
La guarigione delle ferite è un processo fisiologico complesso. Gli scienziati hanno identificato tre fasi generali del processo di guarigione delle ferite: infiammazione, proliferazione e rimodellamento. Ogni fase è caratterizzata da differenze nelle popolazioni cellulari e nelle concentrazioni di citochine, che rappresentano un ambiente chimico-fisiologico unico per un potenziale intervento. Gli studi hanno dimostrato che, sebbene ogni fase del processo di guarigione della ferita sia caratterizzata da diversi sottotipi di cellule cutanee, la maggior parte delle cellule esprime il recettore della melanocortina 1 (MC1R), che lega l'ormone α-melanocito-stimolante. Naturalmente, ciò significa che questi tipi di cellule legano anche gli analoghi dell'α-MSH, come KPV e KdPT.
Poiché questi derivati dell'α-MSH mantengono alcune proprietà dell'α-MSH ma ne mancano altre, sono potenzialmente utili per la guarigione delle ferite. Ad esempio, il KPV possiede le proprietà infiammatorie dell'α-MSH ma manca dell'attività di induzione dei pigmenti del suo peptide progenitore. Ciò rende il KPV un buon candidato per migliorare la guarigione delle ferite evitando i caratteristici cambiamenti cutanei normalmente associati alla formazione di cicatrici naturali (un fenomeno che colpisce in modo sproporzionato gli individui con la pelle più scura).
Una delle ragioni degli effetti antinfiammatori del KPV è il suo coinvolgimento nella risposta immunitaria innata contro due comuni agenti patogeni della pelle. Gli studi hanno dimostrato che il KPV inibisce la crescita dello Staphylococcus aureus e della Candida albicans. Questi benefici si verificano a concentrazioni fisiologiche, il che significa che il KPV può rappresentare un modo efficace per prevenire le infezioni in ferite gravi come le ustioni. Questo beneficio del KPV contrasta con altri farmaci antinfiammatori, che in realtà inibiscono la capacità dell'organismo di combattere le infezioni. Pertanto, KPV combina l'attività antinfiammatoria con quella antimicrobica.
Il KPV è in realtà un modello strutturale in studi recenti che mirano a replicare gli effetti antimicotici dei peptidi in nuove terapie. L'idea è che la struttura 3D del KPV lo renda un potente agente antimicotico, e replicare questa struttura potrebbe consentire ai ricercatori di sviluppare composti con la stessa attività antimicotica ma con effetti diversi su altri processi biologici.
Formazione di cicatrici
Sulla base dei noti benefici della KPV nel primo stadio della guarigione delle ferite (infiammazione), lo studio ha analizzato il suo ruolo anche negli altri due stadi della guarigione delle ferite.La KPV sembra ridurre l'infiammazione cronica che porta alla formazione di cicatrici ipertrofiche (es. cicatrici). Questo tipo di formazione cicatriziale è caratterizzata da un'estesa infiltrazione di macrofagi, immunoreattività al TNF e abbondanza di neutrofili. L'uso di α-MSH in questo contesto produce cicatrici più piccole e una risposta infiammatoria meno drammatica. Effetti simili sono stati riscontrati in altri tessuti, come i polmoni e il cuore. Questi risultati fanno sperare che il KPV possa essere usato per prevenire le cicatrici che si verificano con alcuni farmaci chemioterapici, il che non solo riduce gli effetti collaterali dei trattamenti antitumorali, ma aumenta anche la concentrazione di questi farmaci, migliorando così l'efficacia dei trattamenti antitumorali.
Citazioni di riferimento
- M. E. Hiltz e J. M. Lipton, "Attività antinfiammatoria di un frammento COOH-terminale del neuropeptide alfa-MSH". FASEB J. Off. Publ. Fed. Am. Soc. Exp. Biol., vol. 3, n. 11, pp. 2282-2284, settembre 1989.
- K. Kannengiesser e altri., "Il tripeptide KPV derivato dalla melanocortina ha un potenziale antinfiammatorio in modelli murini di malattia infiammatoria intestinale". Inflamm. Bowel Dis., vol. 14, no. 3, pp. 324-331, marzo 2008, doi: 10.1002/ibd.20334.
- B. Xiao e altri., "La somministrazione mirata per via orale del tripeptide KPV tramite nanoparticelle funzionalizzate con acido ialuronico allevia efficacemente la colite ulcerosa". Mol. Ther. J. Am. Soc. Gene Ther., vol. 25, n. 7, pp. 1628-1640, 05 2017, doi: 10.1016/j.ymthe.2016.11.020.
- G. Dalmasso, L. Charrier-Hisamuddin, H. T. T. Nguyen, Y. Yan, S. Sitaraman e D. Merlin, "L'assorbimento di PepT1-Mediated Tripeptide KPV riduce l'infiammazione intestinale". Gastroenterologia, vol. 134, n. 1, pp. 166-178, gennaio 2008, doi: 10.1053/j.gastro.2007.10.026.
- D. B. Richards e J. M. Lipton, "Effetto dell'alfa-MSH 11-13 (lisina-prolina-valina) sulla febbre nel coniglio". Peptidi, vol. 5, no. 4, pp. 815-817, agosto 1984, doi: 10.1016/0196-9781(84)90027-5.
- T. Brzoska, T. A. Luger, C. Maaser, C. Abels e M. Böhm, "Ormone alfa-melanocito-stimolante e tripeptidi correlati: biochimica, effetti antinfiammatori e protettivi in vitro e in vivo e prospettive future per il trattamento delle malattie infiammatorie immuno-mediate". Endocr. Rev., vol. 29, no. 5, pp. 581-602, agosto 2008, doi: 10.1210/er.2007-0027.
- T. A. Luger e T. Brzoska, "Peptidi correlati all'α-MSH: una nuova classe di farmaci antinfiammatori e immunomodulanti". Ann. Rheum. Dis., vol. 66, no. Suppl 3, pp. iii52-iii55, novembre 2007, doi: 10.1136/ard.2007.079780.
- M. Cutuli, S. Cristiani, J. M. Lipton e A. Catania, "Effetti antimicrobici dei peptidi alfa-MSH". J. Leukoc. Biol., vol. 67, n. 2, pp. 233-239, febbraio 2000, doi: 10.1002/jlb.67.2.233.
- M. F. Masman e altri., "Sintesi e analisi conformazionale di His-Phe-Arg-Trp-NH2 e di analoghi con proprietà antifungine". Bioorg. Med. Chem., vol. 14, n. 22, pp. 7604-7614, novembre 2006, doi: 10.1016/j.bmc.2006.07.007.
- K. S. de Souza e altri., "Miglioramento della guarigione delle ferite cutanee dopo l'iniezione intraperitoneale di ormone alfa-melanocito-stimolante". Exp. Dermatol., vol. 24, no. 3, pp. 198-203, mar. 2015, doi: 10.1111/exd.12609.
- C. Lonati e altri., "Effetti modulatori di NDP-MSH nel fegato in rigenerazione dopo epatectomia parziale nei ratti". Peptidi, vol. 50, pp. 145-152, dicembre 2013, doi: 10.1016/j.peptides.2013.10.014.
- G. Colombo e altri., "Il profilo di espressione genica rivela molteplici influenze protettive del peptide ormone alfa-melanocito-stimolante nel trapianto cardiaco sperimentale". J. Immunol. Baltim. Md 1950, vol. 175, no. 5, pp. 3391-3401, settembre 2005, doi: 10.4049/jimmunol.175.5.3391.
- G. Colombo e altri., "Produzione ed effetti dell'ormone alfa-melanocito-stimolante durante il danno polmonare acuto". Scossa Augusta Ga, vol. 27, no. 3, pp. 326-333, marzo 2007, doi: 10.1097/01.shk.0000239764.80033.7e.
- M. Schiller e altri., "I fibroblasti cutanei umani esprimono le proormone convertasi 1 e 2 e producono peptidi derivati dalla propiomelanocortina". J. Invest. Dermatol., vol. 117, n. 2, pp. 227-235, agosto 2001, doi: 10.1046/j.0022-202x.2001.01412.x.
- T. Brzoska, M. Böhm, A. Lügering, K. Loser e T. A. Luger, "Segnale terminale: effetti antinfiammatori dei peptidi correlati all'ormone α-melanocitario oltre il farmacoforo". Adv. Exp. Med. Biol., vol. 681, pp. 107-116, 2010, doi: 10.1007/978-1-4419-6354-3_8.
- S. J. Getting, H. B. Schiöth, e M. Perretti, "Dissezione dell'effetto antinfiammatorio del nucleo e del C-terminale (KPV) dei peptidi dell'ormone alfa-melanocito-stimolante". J. Pharmacol. Exp. Ther., vol. 306, n. 2, pp. 631-637, agosto 2003, doi: 10.1124/jpet.103.051623.
- K. Pawar, C. S. Kolli, V. K. Rangari e R. J. Babu, "Consegna transdermica iontoforetica del peptide lisina-prolina-valina (KPV) attraverso la pelle umana microporata". J. Pharm. Sci., vol. 106, n. 7, pp. 1814-1820, luglio 2017, doi: 10.1016/j.xphs.2017.03.017.
TUTTI GLI ARTICOLI E LE INFORMAZIONI SUI PRODOTTI FORNITI IN QUESTO SITO WEB SONO SOLO A SCOPO INFORMATIVO ED EDUCATIVO.
In nessun modo questo medico/scienziato approva o sostiene l'acquisto, la vendita o l'uso di questo prodotto per qualsiasi motivo. MOL Changes non ha alcuna affiliazione o relazione, implicita o meno, con questo medico. Lo scopo di citare questo medico è quello di riconoscere e lodare l'esauriente lavoro di ricerca e sviluppo svolto dagli scienziati che lavorano su questo peptide.
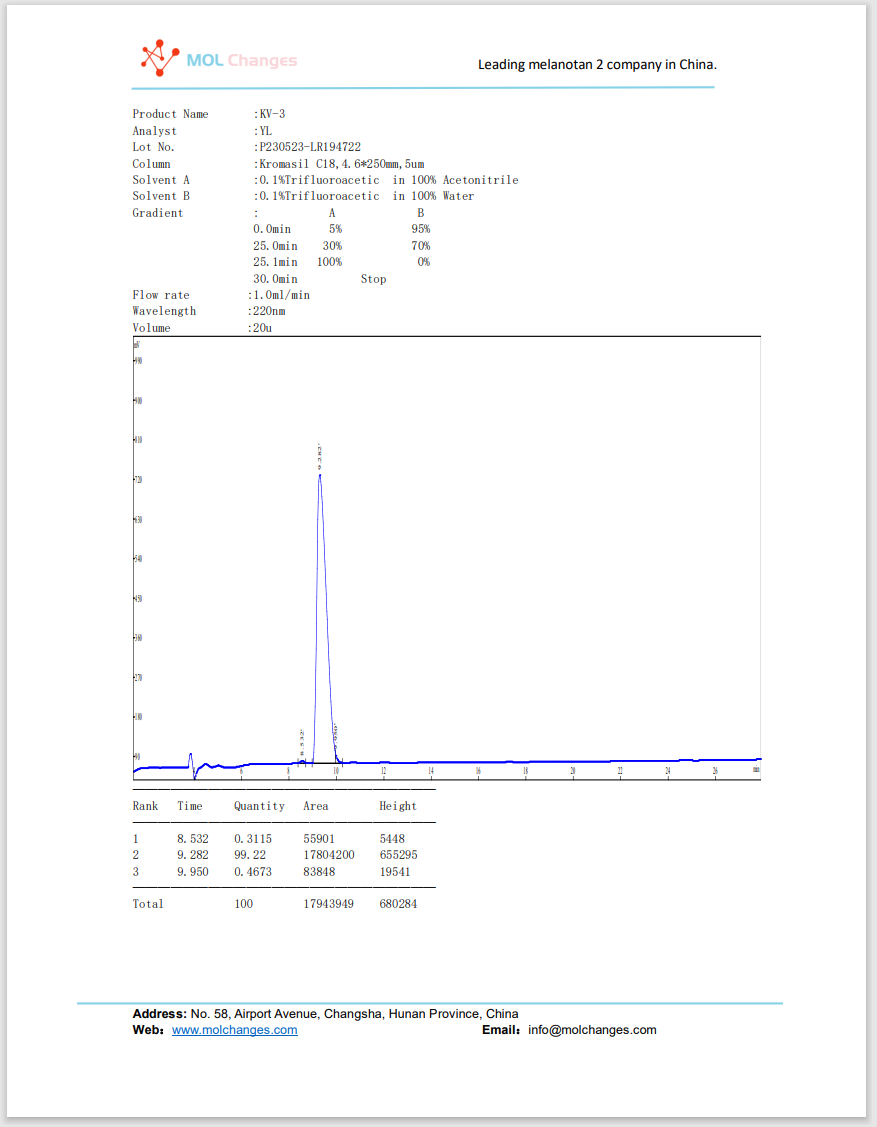
Rapporto di prova HPLC
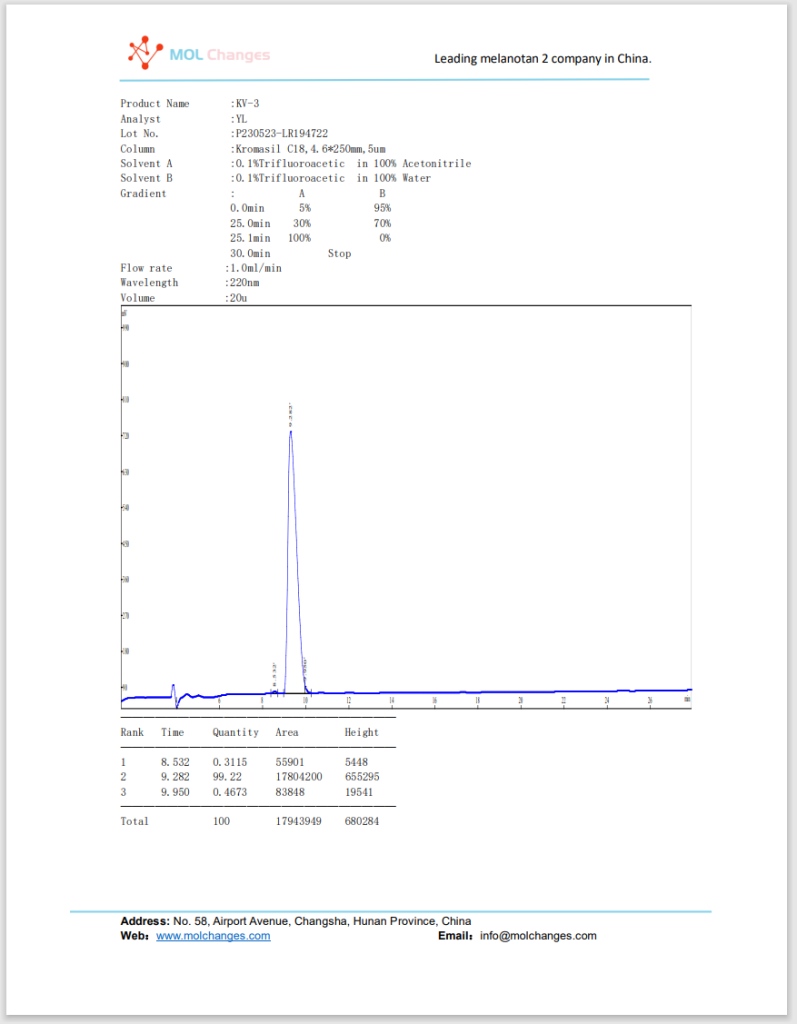
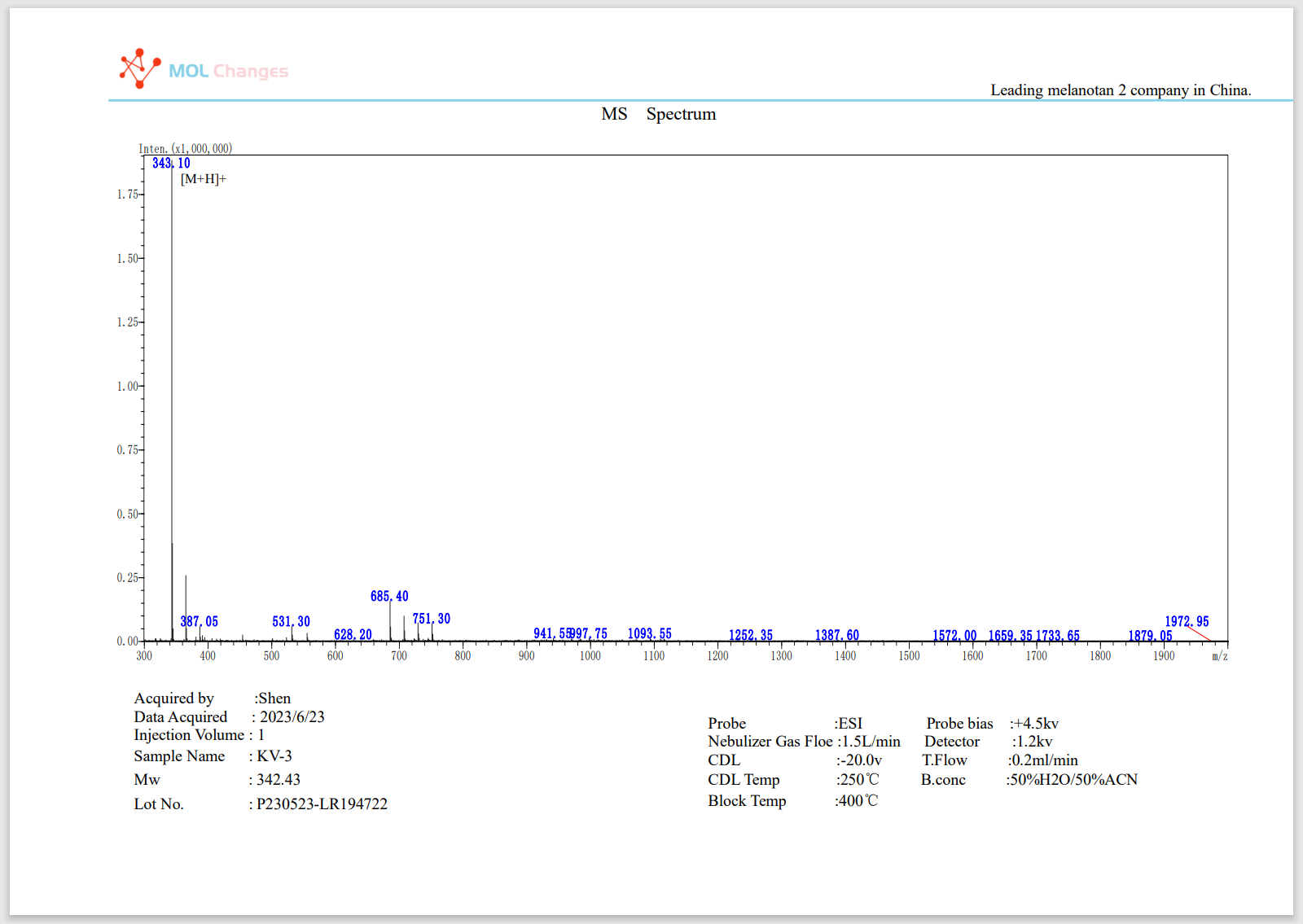
Rapporto di prova MS
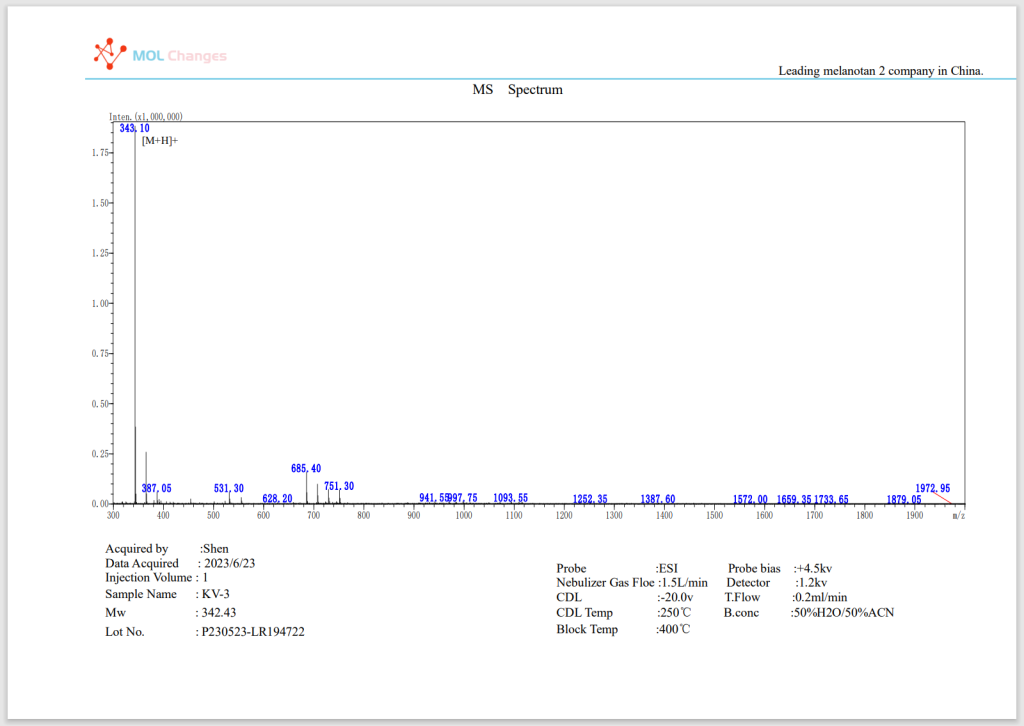
Informazioni sul produttore
- KPV è prodotto dalla fabbrica MOL Changes.
- Fornitore di KPV Cambiamenti di MOL.
- Volume di produzione massimo accettabile: 100000 bottiglie.
- Contenuto standard: peptide netto.
- Purezza: ≥98% per tutti i prodotti.
- Personalizzazione: La personalizzazione delle dimensioni di 1mg-1g è accettabile