KPV
O KPV tem uma potente atividade anti-inflamatória no sistema nervoso central, no trato gastrointestinal, nos pulmões, no sistema vascular e nas articulações.
$4.10
WhatsApp-nos
◐ Preço por atacado no WhatsApp!
◐ MOQ: 10 peças
◐ Fábrica de fabrico de péptidos
◐ Implementação das normas CGMP
◐ ISO9001 E ISO14000
PARTILHAR
Navegação de informações sobre produtos
Estrutura do KPV
- Sequência:Lys-Pro-Val
- Número CAS:67727-97-3
- Fórmula molecular:C16H30N4O4
- Peso molecular: 342,43 g/mol
O que é o KPV?
O KPV é um fragmento peptídico C-terminal da hormona estimuladora de α-melanócitos (α-MSH). É um dos vários derivados peptídicos curtos da α-MSH que foram testados para determinar se mantêm propriedades fotoprotectoras semelhantes, atividade anti-isquémica, efeitos sexuais ou benefícios no comportamento alimentar e na homeostase energética.
O KPV é constituído por lisina-prolina-valina e tem propriedades anti-inflamatórias significativas, estando o péptido a ser ativamente investigado como uma potencial terapia para a doença inflamatória intestinal. Há provas de uma potente atividade anti-inflamatória no sistema nervoso central, no trato gastrointestinal, nos pulmões, no sistema vascular e nas articulações e, como o KPV é um pequeno péptido, pode ser administrado de várias formas, incluindo por via oral, intravenosa e transdérmica.
Efeitos do KPV
Inflamação intestinal
Talvez a descoberta mais importante na investigação do KPV seja o facto de o péptido reduzir a inflamação intestinal. Num modelo de ratinho de doença inflamatória intestinal (DII), o KPV mostrou resultados robustos na redução dos infiltrados inflamatórios, da atividade da MPO e da evidência histológica geral de inflamação, e os ratinhos tratados com KPV no estudo recuperaram mais rapidamente e ganharam mais peso do que os ratinhos tratados com placebo.
Outros estudos sobre o mecanismo de administração do KPV demonstraram que o carregamento do KPV em nanopartículas funcionalizadas com ácido hialurónico ajuda a dirigir os efeitos inflamatórios do péptido para os locais apropriados no intestino. Em modelos de ratinhos, este facto acelera a cicatrização da mucosa e reduz a inflamação através de uma forte regulação negativa do TNF-α. Em muitos aspectos, o KPV é uma abordagem mais eficaz e direccionada para reduzir a inflamação da DII sem afetar o TNF-α noutras partes do organismo. A modificação do KPV tem a vantagem de aumentar a biodisponibilidade oral do péptido. Isto não aumenta a eficácia do péptido, mas afecta a potência, bem como a dose total necessária para atingir o efeito.
A KPV parece ser eficaz apenas em casos de inflamação excessiva. Tem pouco ou nenhum efeito nos tecidos normais. Isto deve-se, pelo menos em parte, ao facto de o KPV entrar nas células do cólon através de proteínas de transporte que não são reguladas em situações inflamatórias. Isto sugere que o KPV pode ser um medicamento profilático ou de manutenção eficaz para a DII. É seguro tomá-lo mesmo durante o período de repouso porque não tem qualquer efeito. Didier Merlin, que conduziu uma série de estudos sobre os potenciais benefícios gastrointestinais do KPV, descobriu recentemente que o péptido entra nas células do cólon através do PepT1, um canal proteico que só é expresso em quantidade real no intestino durante estados inflamatórios. Este facto ajuda a explicar porque é que o KPV é mais eficaz num ambiente já inflamado. Sugere também um novo modo de administração de medicamentos que pode ser aplicado a uma vasta gama de doenças. Ao visar proteínas que são alteradas em condições de doença, mesmo que não sejam diretamente causadoras de doença, é possível concentrar a atividade de um medicamento em determinadas regiões. Isto poderia reduzir a dosagem de medicamentos com efeitos secundários graves e desenvolver medicamentos que, embora não sejam eficazes por si só, têm um poderoso efeito terapêutico no estado de doença correto.
KPV como anti-inflamatório geral
Já em 1984, estudos efectuados em coelhos demonstraram que o KPV era um potente anti-inflamatório e antipirético (redutor da febre). No entanto, neste caso, o KPV era menos potente do que a molécula de α-MSH intacta. Isto indicou aos cientistas da época que o KPV não possuía certas partes da molécula α-MSH necessárias para uma atividade antipirética completa [5]. Seguiram-se décadas de investigação de várias formas modificadas de α-MSH.
Talvez a maior lição aprendida com estes testes seja que tanto a α-MSH como vários dos seus análogos reduzem a inflamação numa vasta gama de doenças. Até à data, estas moléculas foram testadas na febre, na dermatite de contacto irritante e alérgica, na vasculite, na fibrose, na artrite e na inflamação dos olhos, do cérebro, dos pulmões e do trato gastrointestinal. Em todos os casos, a alfa-MSH é o agente anti-inflamatório mais eficaz. Infelizmente, tem um efeito secundário importante - provoca a pigmentação da pele. O KPV, por outro lado, não tem este efeito secundário. Embora o KPV não seja tão eficaz como a α-MSH intacta, a sua ausência de efeitos secundários significa que é teoricamente possível aumentar os níveis para atingir o efeito desejado na maioria dos casos.
Verificou-se que as diferenças de potência são mínimas, na melhor das hipóteses, uma vez que a maioria dos efeitos anti-inflamatórios da α-MSH se deve, na realidade, à fração KPV. Curiosamente, no entanto, a molécula-mãe parece ser mais capaz de inibir as respostas inflamatórias tardias. Por exemplo, na dermatite de contacto, a α-MSH previne melhor as reacções inflamatórias alérgicas até 2 semanas após a exposição inicial. Isto sugere que a α-MSH pode influenciar algum aspeto da regulação imunitária que não está relacionado com a resposta inflamatória imediata [7]. Ainda está a ser determinado qual é este processo.
Esta figura mostra o inchaço do ouvido devido a dermatite de contacto às 24 horas (esquerda) e às 2 semanas (direita). Note-se que, às 24 horas, a coadministração de KPV com o estímulo é quase tão eficaz como a coadministração de α-MSH com o estímulo. No entanto, ao fim de 2 semanas, a exposição ao irritante sem a coadministração do péptido resultou num inchaço muito menor da α-MSH em comparação com a KPV.
Cicatrização de feridas
A cicatrização de feridas é um processo fisiológico complexo. Os cientistas identificaram três fases gerais do processo de cicatrização de feridas: inflamação, proliferação e remodelação. Cada fase é caracterizada por diferenças nas populações celulares e nas concentrações de citocinas, representando um ambiente químico/fisiológico único para uma potencial intervenção. Estudos demonstraram que, embora cada fase do processo de cicatrização de feridas seja caracterizada por diferentes subtipos de células da pele, a maioria das células expressa o recetor da melanocortina 1 (MC1R), que se liga à hormona estimuladora dos melanócitos α. Naturalmente, isto também significa que estes tipos de células também se ligam a análogos da α-MSH, como a KPV e a KdPT.
Uma vez que estes derivados da α-MSH mantêm algumas das propriedades da α-MSH, mas carecem de outras, são potencialmente benéficos na cicatrização de feridas. Por exemplo, o KPV fornece as propriedades inflamatórias da α-MSH, mas não possui a atividade indutora de pigmentação do seu peptídeo de origem. Isto torna o KPV um bom candidato para melhorar a cicatrização de feridas, evitando as alterações cutâneas características normalmente associadas à formação natural de cicatrizes (um fenómeno que afecta desproporcionadamente os indivíduos de pele mais escura).
Uma das razões para os efeitos anti-inflamatórios do KPV é o seu envolvimento na resposta imunitária inata contra dois agentes patogénicos comuns da pele. Estudos demonstraram que o KPV inibe o crescimento de Staphylococcus aureus e Candida albicans. Estes benefícios ocorrem em concentrações fisiológicas, o que significa que o KPV pode constituir uma forma eficaz de prevenir infecções em feridas graves, como queimaduras. Este benefício do KPV contrasta com outros medicamentos anti-inflamatórios, que na realidade inibem a capacidade do organismo para combater infecções. Assim, o KPV combina a atividade anti-inflamatória com a atividade antimicrobiana.
O KPV é, na verdade, um modelo estrutural em estudos recentes que visam replicar os efeitos antifúngicos dos péptidos em novas terapêuticas. A ideia é que a estrutura 3D do KPV faz dele um potente agente antifúngico, e replicar esta estrutura pode permitir aos investigadores desenvolver compostos que tenham a mesma atividade antifúngica mas efeitos diferentes noutros processos biológicos.
Formação de cicatrizes
Com base nos benefícios conhecidos do KPV na primeira fase da cicatrização de feridas (inflamação), o estudo também investigou o seu papel nas outras duas fases da cicatrização de feridas. O KPV parece reduzir a inflamação crónica que leva à formação de cicatrizes hipertróficas (por exemplo, cicatrizes). Este tipo de formação de cicatrizes é caracterizado por uma extensa infiltração de macrófagos, imunoreactividade do TNF e abundância de neutrófilos. A utilização de α-MSH neste contexto resulta em cicatrizes mais pequenas e numa resposta inflamatória menos dramática. Foram encontrados efeitos semelhantes noutros tecidos, como os pulmões e o coração. Estas descobertas dão esperança de que o KPV possa ser utilizado para prevenir as cicatrizes observadas com certos medicamentos quimioterapêuticos, o que não só reduz os efeitos secundários dos tratamentos contra o cancro, mas também aumenta a concentração destes medicamentos, melhorando assim a eficácia dos tratamentos contra o cancro.
Citações referenciadas
- M. E. Hiltz e J. M. Lipton, "Antiinflammatory activity of a COOH-terminal fragment of the neuropeptide alpha-MSH," FASEB J. Off. Publ. Fed. Am. Soc. Exp. Biol., vol. 3, no. 11, pp. 2282-2284, Sep. 1989.
- K. Kannengiesser et al., "O tripeptídeo KPV derivado da melanocortina tem potencial anti-inflamatório em modelos murinos de doença inflamatória intestinal," Inflamm. Bowel Dis., vol. 14, no. 3, pp. 324-331, Mar. 2008, doi: 10.1002/ibd.20334.
- B. Xiao et al., "Orally Targeted Delivery of Tripeptide KPV via Hyaluronic Acid-Functionalized Nanoparticles Efficiently Alleviates Ulcerative Colitis," (Entrega do tripeptídeo KPV por via oral através de nanopartículas funcionalizadas com ácido hialurónico) Mol. Ther. J. Am. Soc. Gene Ther., vol. 25, no. 7, pp. 1628-1640, 05 2017, doi: 10.1016/j.ymthe.2016.11.020.
- G. Dalmasso, L. Charrier-Hisamuddin, H. T. T. Nguyen, Y. Yan, S. Sitaraman, e D. Merlin, "PepT1-Mediated Tripeptide KPV Uptake Reduces Intestinal Inflammation," Gastroenterologia, vol. 134, no. 1, pp. 166-178, Jan. 2008, doi: 10.1053/j.gastro.2007.10.026.
- D. B. Richards e J. M. Lipton, "Effect of alpha-MSH 11-13 (lysine-proline-valine) on fever in the rabbit," (Efeito da alfa-MSH 11-13 (lisina-prolina-valina) na febre do coelho). Péptidos, vol. 5, no. 4, pp. 815-817, Aug. 1984, doi: 10.1016/0196-9781(84)90027-5.
- T. Brzoska, T. A. Luger, C. Maaser, C. Abels, e M. Böhm, "Alpha-melanocyte-stimulating hormone and related tripeptides: biochemistry, antiinflammatory and protective effects in vitro and in vivo, and future perspectives for the treatment of immune-mediated inflammatory diseases," Endocr. Rev., vol. 29, no. 5, pp. 581-602, Aug. 2008, doi: 10.1210/er.2007-0027.
- T. A. Luger e T. Brzoska, "α-MSH related peptides: a new class of anti-inflammatory and immunomodulating drugs," Ann. Rheum. Dis., vol. 66, no. Suppl 3, pp. iii52-iii55, Nov. 2007, doi: 10.1136/ard.2007.079780.
- M. Cutuli, S. Cristiani, J. M. Lipton, e A. Catania, "Antimicrobial effects of alpha-MSH peptides," J. Leukoc. Biol., vol. 67, no. 2, pp. 233-239, Fev. 2000, doi: 10.1002/jlb.67.2.233.
- M. F. Masman et al., "Síntese e análise conformacional de His-Phe-Arg-Trp-NH2 e análogos com propriedades antifúngicas," Bioorg. Med. Chem., vol. 14, no. 22, pp. 7604-7614, Nov. 2006, doi: 10.1016/j.bmc.2006.07.007.
- K. S. de Souza et al., "Melhoria da cicatrização de feridas cutâneas após injeção intraperitoneal de hormona estimuladora de alfa-melanócitos," Exp. Dermatol., vol. 24, no. 3, pp. 198-203, Mar. 2015, doi: 10.1111/exd.12609.
- C. Lonati et al., "Efeitos moduladores da NDP-MSH na regeneração do fígado após hepatectomia parcial em ratos," Péptidos, vol. 50, pp. 145-152, Dez. 2013, doi: 10.1016/j.peptides.2013.10.014.
- G. Colombo et al., "Gene expression profiling reveals multiple protective influences of the peptide alpha-melanocyte-stimulating hormone in experimental heart transplantation," J. Immunol. Baltim. Md 1950, vol. 175, no. 5, pp. 3391-3401, Sep. 2005, doi: 10.4049/jimmunol.175.5.3391.
- G. Colombo et al., "Production and effects of alpha-melanocyte-stimulating hormone during acute lung injury," Choque Augusta Ga, vol. 27, no. 3, pp. 326-333, Mar. 2007, doi: 10.1097/01.shk.0000239764.80033.7e.
- M. Schiller et al., "Human Dermal Fibroblasts Express Prohormone Convertases 1 and 2 and Produce Proopiomelanocortin-Derived Peptides," J. Invest. Dermatol., vol. 117, no. 2, pp. 227-235, Aug. 2001, doi: 10.1046/j.0022-202x.2001.01412.x.
- T. Brzoska, M. Böhm, A. Lügering, K. Loser e T. A. Luger, "Terminal signal: anti-inflammatory effects of α-melanocyte-stimulating hormone related peptides beyond the pharmacophore," (Sinal terminal: efeitos anti-inflamatórios dos péptidos relacionados com a hormona estimuladora de melanócitos α para além do farmacóforo). Adv. Exp. Med. Biol., vol. 681, pp. 107-116, 2010, doi: 10.1007/978-1-4419-6354-3_8.
- S. J. Getting, H. B. Schiöth e M. Perretti, "Dissecação do efeito anti-inflamatório dos péptidos da hormona estimuladora de alfa-melanócitos do núcleo e do terminal C (KPV)," J. Pharmacol. Exp. Ther., vol. 306, no. 2, pp. 631-637, Aug. 2003, doi: 10.1124/jpet.103.051623.
- K. Pawar, C. S. Kolli, V. K. Rangari, e R. J. Babu, "Transdermal Iontophoretic Delivery of Lysine-Proline-Valine (KPV) Peptide Across Microporated Human Skin," J. Pharm. Sci., vol. 106, no. 7, pp. 1814-1820, Jul. 2017, doi: 10.1016/j.xphs.2017.03.017.
TODOS OS ARTIGOS E INFORMAÇÕES SOBRE PRODUTOS FORNECIDOS NESTE SÍTIO WEB DESTINAM-SE APENAS A FINS INFORMATIVOS E EDUCATIVOS.
De forma alguma este médico/cientista endossa ou defende a compra, venda ou uso deste produto por qualquer motivo. A MOL Changes não tem qualquer afiliação ou relação, implícita ou não, com este médico. O objetivo de citar este médico é reconhecer, reconhecer e elogiar o trabalho exaustivo de investigação e desenvolvimento realizado pelos cientistas que trabalham neste péptido.
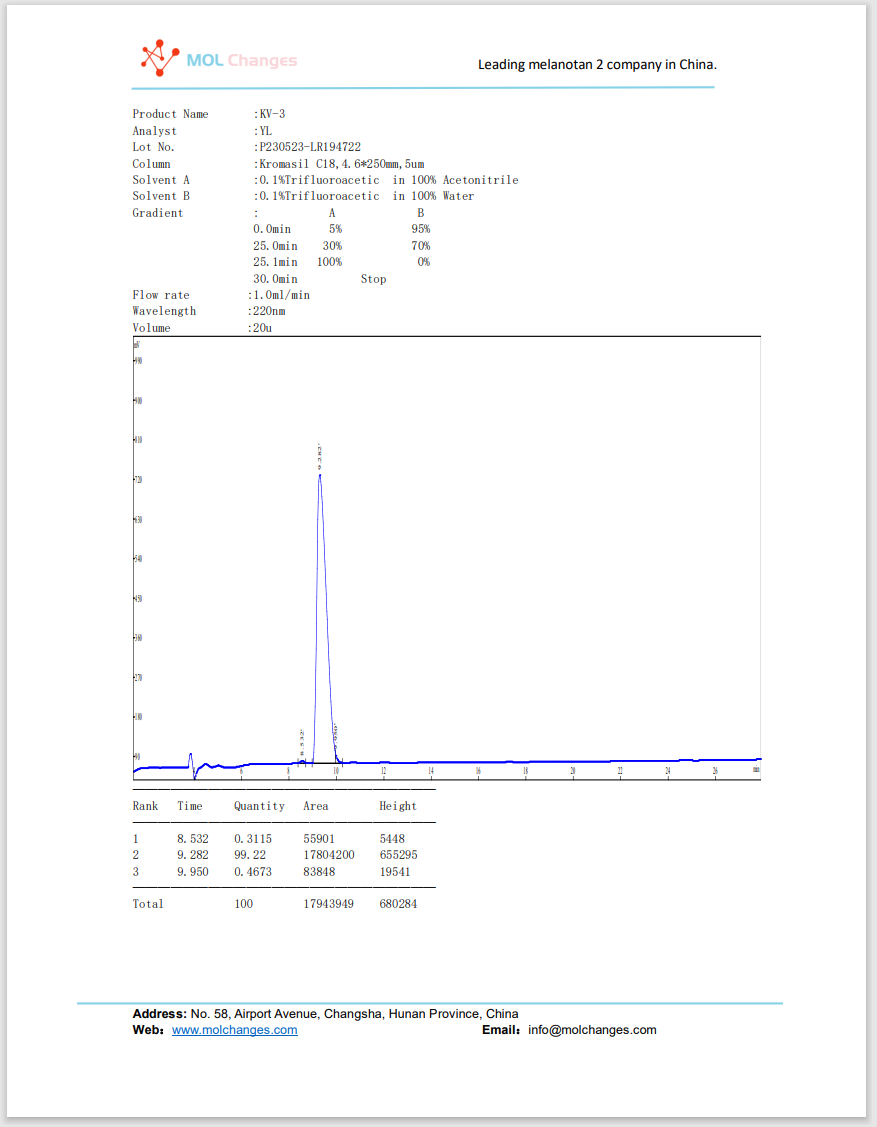
Relatório de ensaio de HPLC
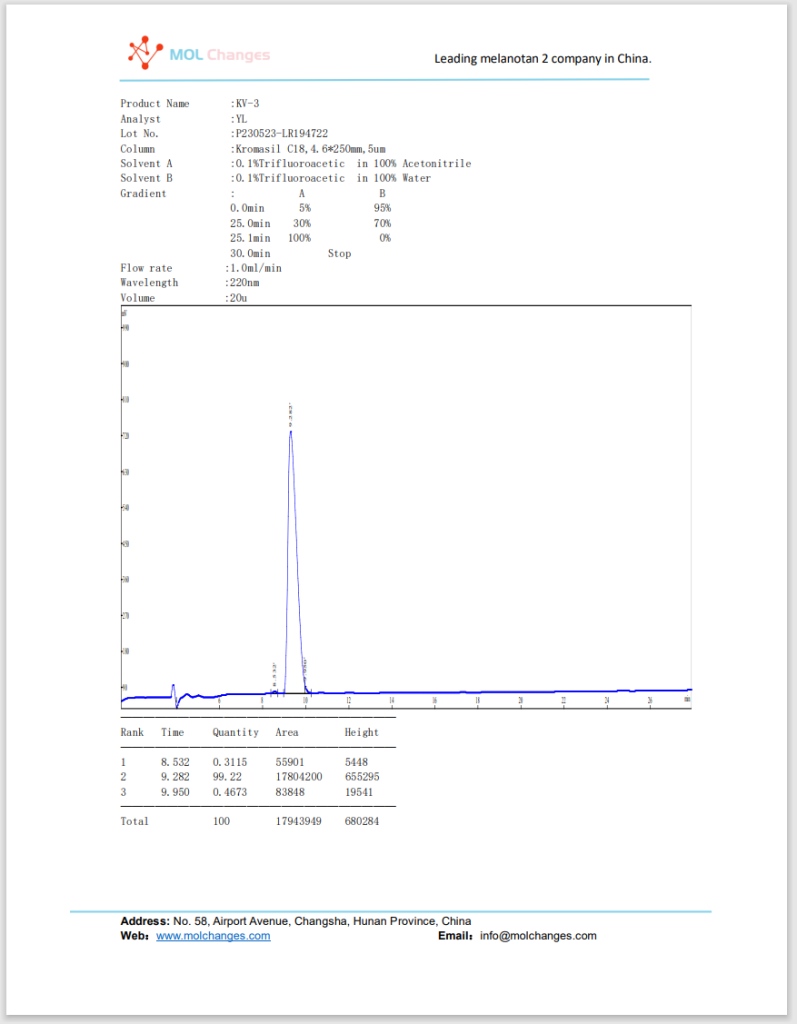
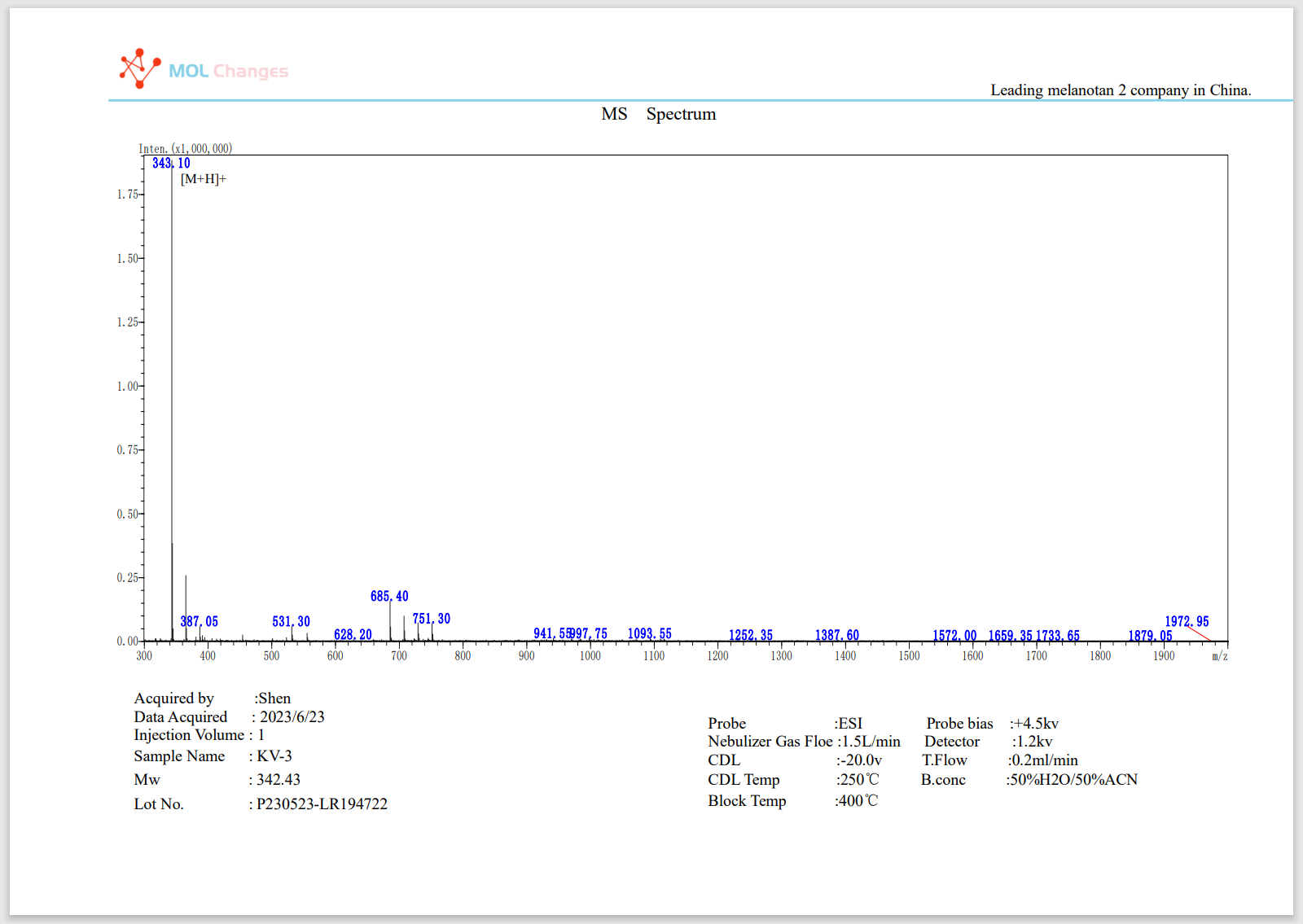
Relatório de ensaio EM
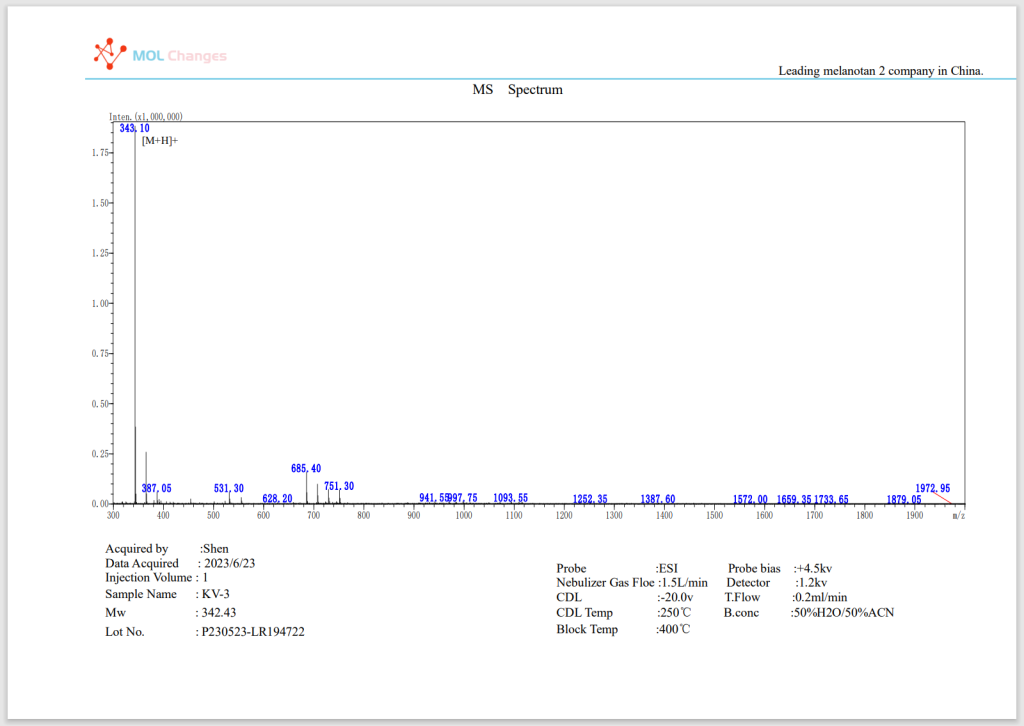
Informações do fabricante
- O KPV é fabricado pela fábrica MOL Changes.
- Mudanças no fornecedor KPV MOL.
- Volume máximo de produção aceitável: 100000 garrafas.
- Norma de conteúdo: péptido líquido.
- Pureza: ≥98% para todos os produtos.
- Personalização: A personalização do tamanho 1mg-1g é aceitável